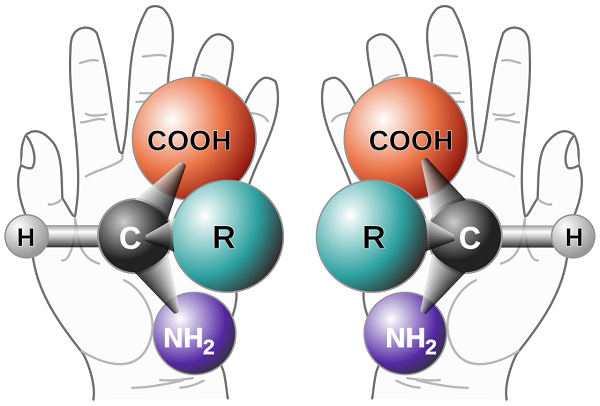
وقتی در مولکولی چهار گروه مختلف به یک اتم کربن متصل باشند، آن کربن، کایرال (مرکز فضایی یا مرکز کایرال) نامیده میشود. به کربن موجود در این نوع مولکولها مرکز کایرال یا کربن نامتقارن نیز میگویند. مرکز کایرال را در متون علمی بهطور قراردادی با ستاره (*) نشان میدهند. رابطهٔ بین انانتیومرها همانند رابطهٔ دست چپ و راست است و در صورتی که چهار گروه مختلف به کربن چهار وجهی متصل باشند، به وجود میآید. مولکول-هایی که حداقل یک مرکز کایرال داشته باشند، بر تصویر آینهای خود قابل انطباق نیستند و به-صورت یک جفت انانتیومر وجود دارند. خصوصیتهای فیزیکی همچون نقطهٔ ذوب، نقطه ی جوش، انحلال پذیری و چگالی یک جفت انانتیومر کاملاً شبیه هم است و به وسیلهٔ این روشها نمیتوان دو ترکیب انانتیومر را از هم جدا کرد.
تقارن در مولکول به تشخیص مولکول کایرال از غیرکایرال (ناکایرال) کمک میکند. مولکول فوق صفحه تقارن دارد. صفحه تقارن صفحهای فرضیاست که از وسط جسم یا مولکول می-گذرد (مانند یک آینه آن را از وسط نصف میکند) و نیمی از جسم یا مولکول را بهصورت تصویر آینهای نیمه دیگر درمیآورد. در واقع صفحه تقارن یکی از عناصر تقارنی است که اگر مولکولی دارای صفحه تفارن باشد، غیرکایرال خواهد بود، همانند مولکول متان. تعداد زیادی از مولکولها رامیتوان با تشخیص صفحه تقارن به مولکولهای کایرال و غیرکایرال دستهبندی کرد. بهطور مثال، یک دست فاقد تقارن است. نصف یک دست، تصویر آیینهای «نیم» دیگر نیست.











 تماس با کارشناسان
تماس با کارشناسان